Design klinické studie
Studie KEYNOTE-581/CLEAR: multicentrická, randomizovaná, otevřená studie zahrnující 1 069 pacientů.
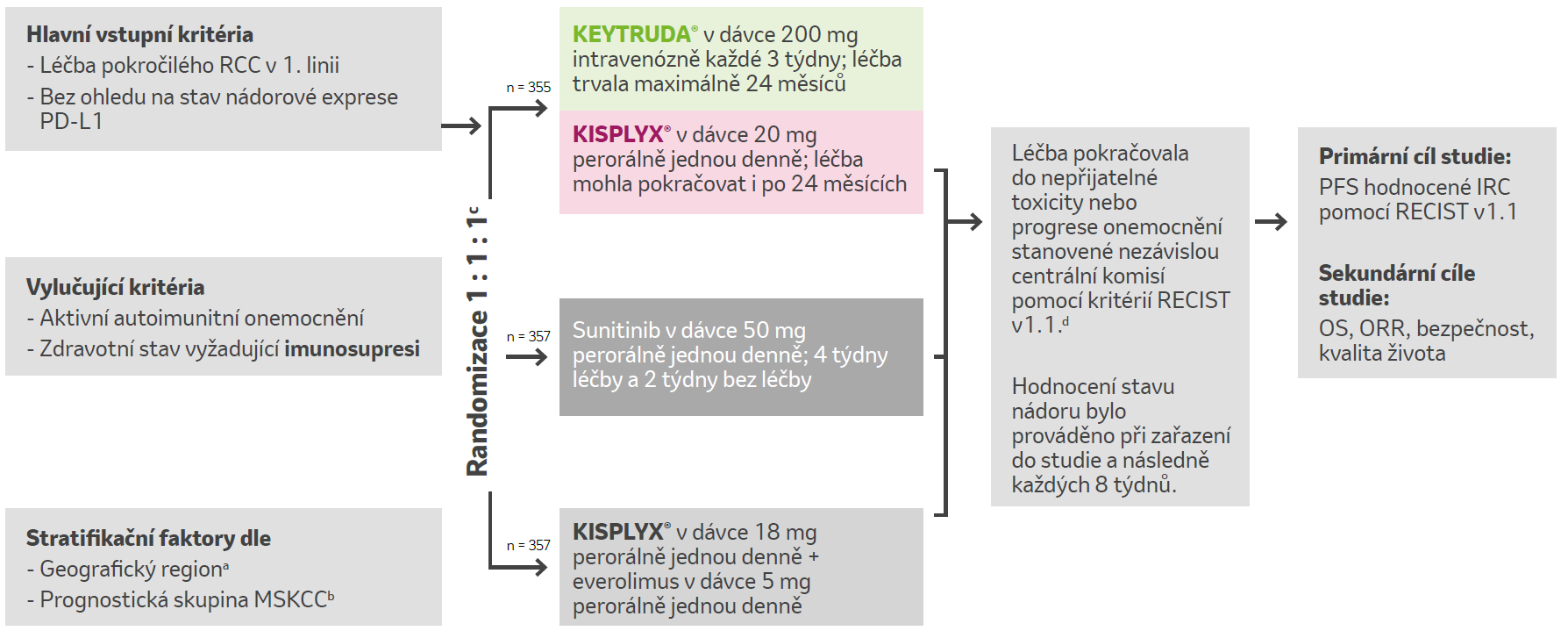
a Severní Amerika a Západní Evropa vs. „zbytek světa“.
b Randomizace byla stratifikovaná podle prognostických skupin Memorial Sloan Kettering Cancer Center (MSKCC): příznivá vs. středně příznivá vs. špatná.
c Klinická data jsou uvedena ze skupiny s přípravky KEYTRUDA® + KISPLYX® a ze skupiny se sunitinibem.
d Podávání kombinace přípravků KEYTRUDA® + KISPLYX® bylo povoleno i po progresi onemocnění definované RECIST, pokud byl pacient klinicky stabilní a pokud zkoušející považoval další léčbu za přínosnou.
Výchozí demografické a klinické charakteristiky ve studii KEYNOTE-581/CLEAR1

Rozložení rizikových skupin ve studii KEYNOTE-581/CLEARa

a Randomizace byla stratifikovaná podle prognostických skupin Memorial Sloan Kettering Cancer Center (MSKCC).
Reference:
1 Motzer R, Alekseev B, Rha S-Y, et al. Lenvatinib plus pembrolizumab or everolimus for advanced renal cell carcinoma. N Engl J Med. 2021;384(14):1289–1300.
2 Motzer R, Alekseev B, Rha S-Y, et al. Supplementary Appendix to: Lenvatinib plus pembrolizumab or everolimus for advanced renal cell carcinoma. N Engl J Med. 2021;384(14):1289–1300. doi:10.1056/NEJMoa2035716.
3 SPC přípravku KEYTRUDA® na www.sukl.cz.