Výsledky klinické studie
Výsledky PFS z předem specifikované finální analýzy OS ze studie KEYNOTE-581/CLEAR1
Medián doby sledování (IQR) pro PFS byl 39,2 měsíce (22,1–48,5) ve skupině léčené kombinací přípravků KEYTRUDA® + KISPLYX® a 20,6 měsíce (5,5–41,2) ve skupině léčené sunitinibem.1
Předem specifikovaná finální analýza OS byla provedena po 23 měsících dalšího sledování od primární analýzy.1
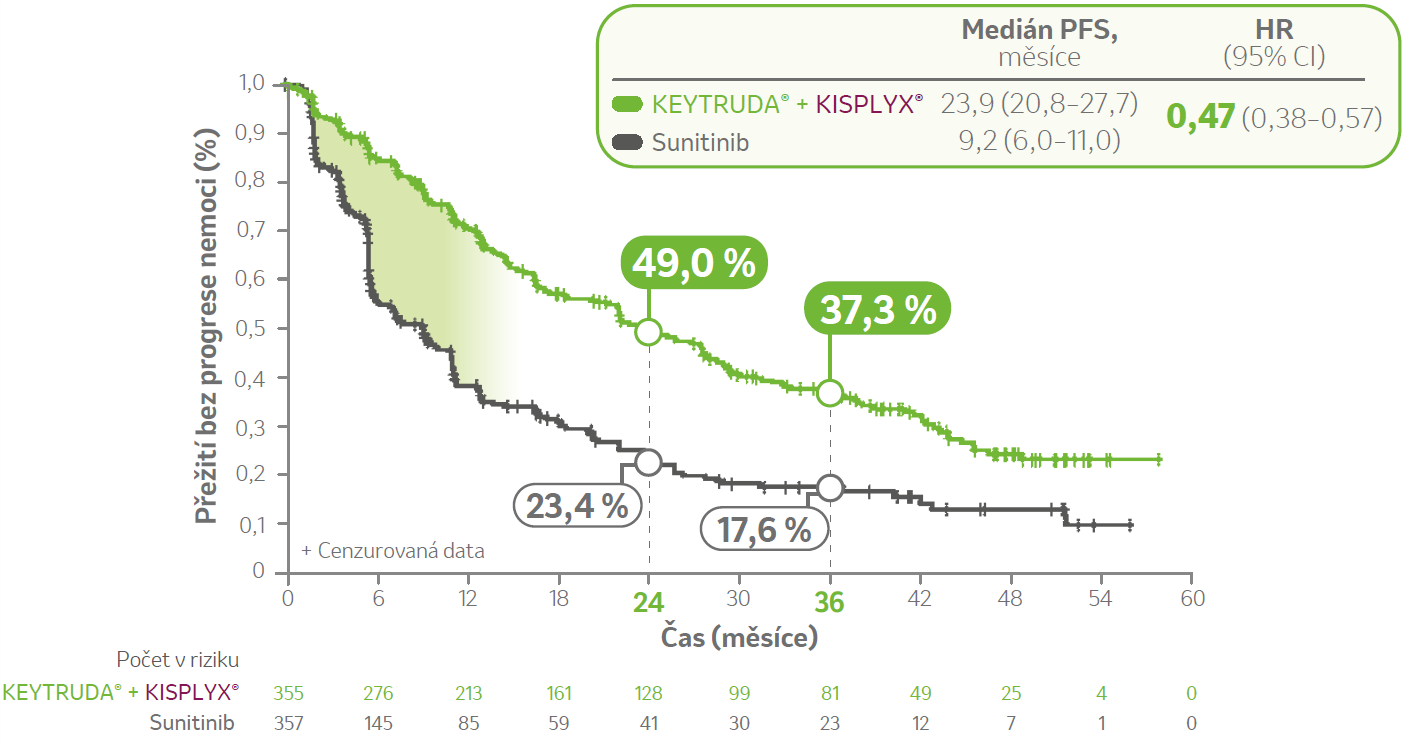
Kombinace přípravků KEYTRUDA® + KISPLYX® více než zdvojnásobila medián PFS v porovnání se sunitinibem (23,9 měsíce vs. 9,2 měsíce)

Hodnota PFS byla stanovena nezávislým přezkoumáním zobrazení podle RECIST v1.1. 95% Cl byly odhadnuty generalizovanou Brookmeyer-Crowley metodou. Poměr rizik byl stanoven na základě Coxova modelu proporcionálních rizik s léčebnou skupinou jako faktorem; pro vazby byla použita Efronova metoda se stratifikací podle geografických regionů (region 1: západní Evropa a Severní Amerika, region 2: zbytek světa) a prognostických skupin podle MSKCC (příznivá, středně příznivá a špatná) v IxRS.1
Analýzy PFS v rizikových podskupinách podle IMDC1
Rizikové skupiny se středně příznivou a špatnou prognózou1
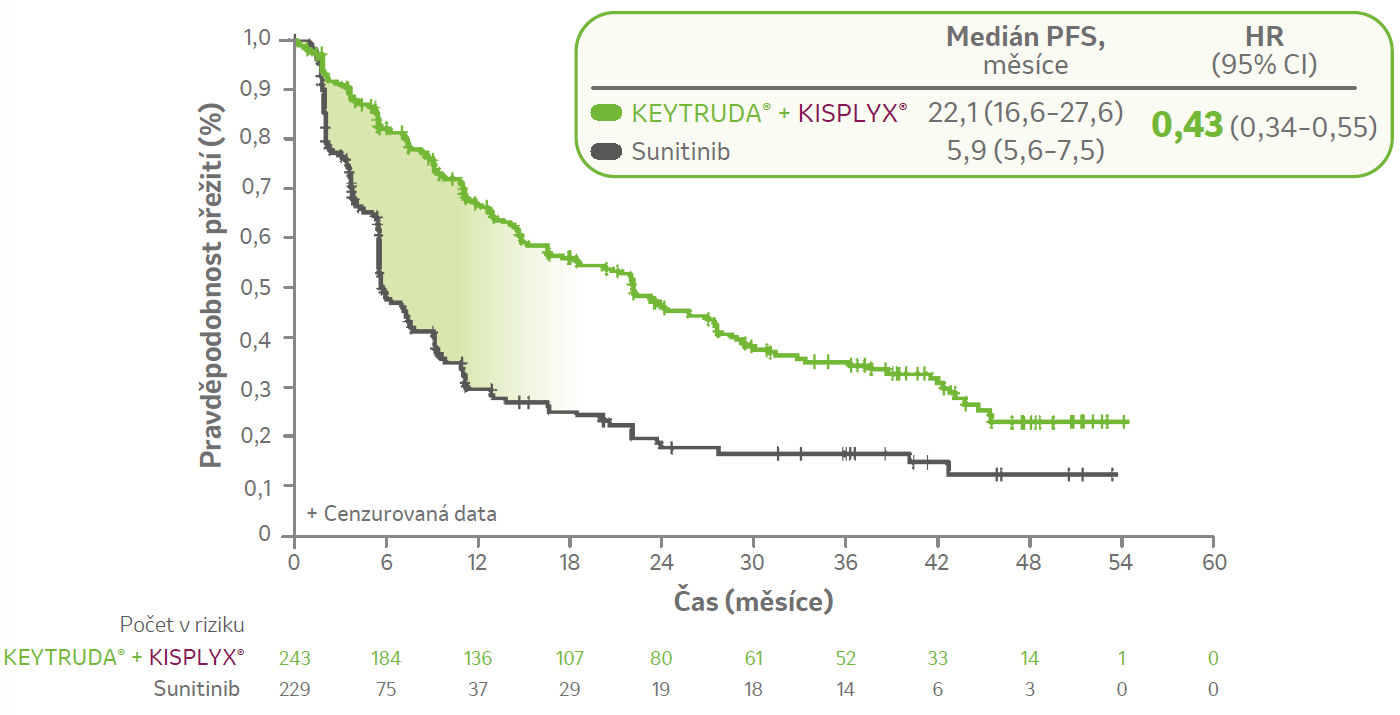
Superiorní PFS v porovnání
se sunitinibem

Hodnota PFS byla stanovena nezávislým přezkoumáním zobrazení podle RECIST v1.1. Riziková skupina podle IMDC nebyla stratifikačním faktorem, relevantní data byla odvozena programově. Mediány byly určeny metodou Kaplan-Meierových odhadů, 95% Cl byly odhadnuty generalizovanou Brookmeyer-Crowley metodou. Poměr rizik byl stanoven na základě Coxova modelu proporcionálních rizik s léčebnou skupinou jako faktorem; pro vazby byla použita Efronova metoda. Stratifikačními faktory byly geografické regiony (region 1: západní Evropa a Severní Amerika, region 2: zbytek světa) a prognostické skupiny podle MSKCC (příznivá, středně příznivá a špatná) v IxRS.1
Předem specifikovaná finální analýza OS ze studie KEYNOTE-581/CLEAR1
Při mediánu doby sledování OS (IQR) 49,8 měsíce (41,4–53,1) ve skupině KEYTRUDA® + KISPLYX® a 49,4 měsíce (41,6–52,8) ve skupině sunitinibu se vyskytlo 308 cílových příhod OS (KEYTRUDA® + KISPLYX®, 149 příhod; sunitinib, 159 příhod).
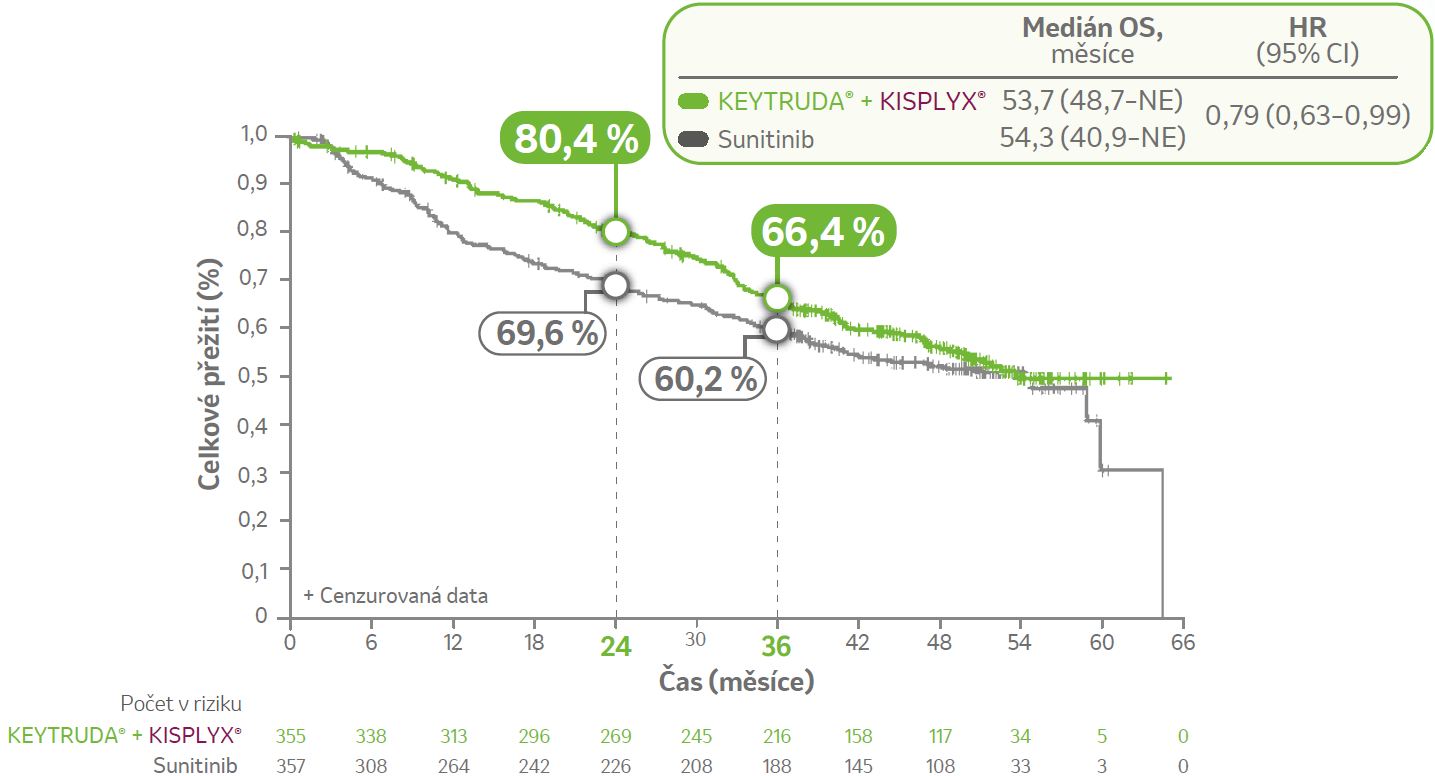

Odhady HR a oboustranného 95% Cl pro léčbu kombinací přípravků KEYTRUDA® + KISPLYX® oproti sunitinibu byly provedeny na základě Coxova modelu proporcionálních rizik s použitím Efronovy metody pro vazby a se stratifikací podle geografického regionu a prognostických skupin dle MSKCC.
Finální analýza OS adjustovaná o následné léčby protinádorovými léčivými přípravky1
Méně pacientů v rameni KEYTRUDA® + KISPLYX® (15,8 %) dostalo jako následnou protinádorovou léčbu inhibitory kontrolních bodů PD-1/PD-L1 ve srovnání v rameni se sunitinibem (54,6 %).1
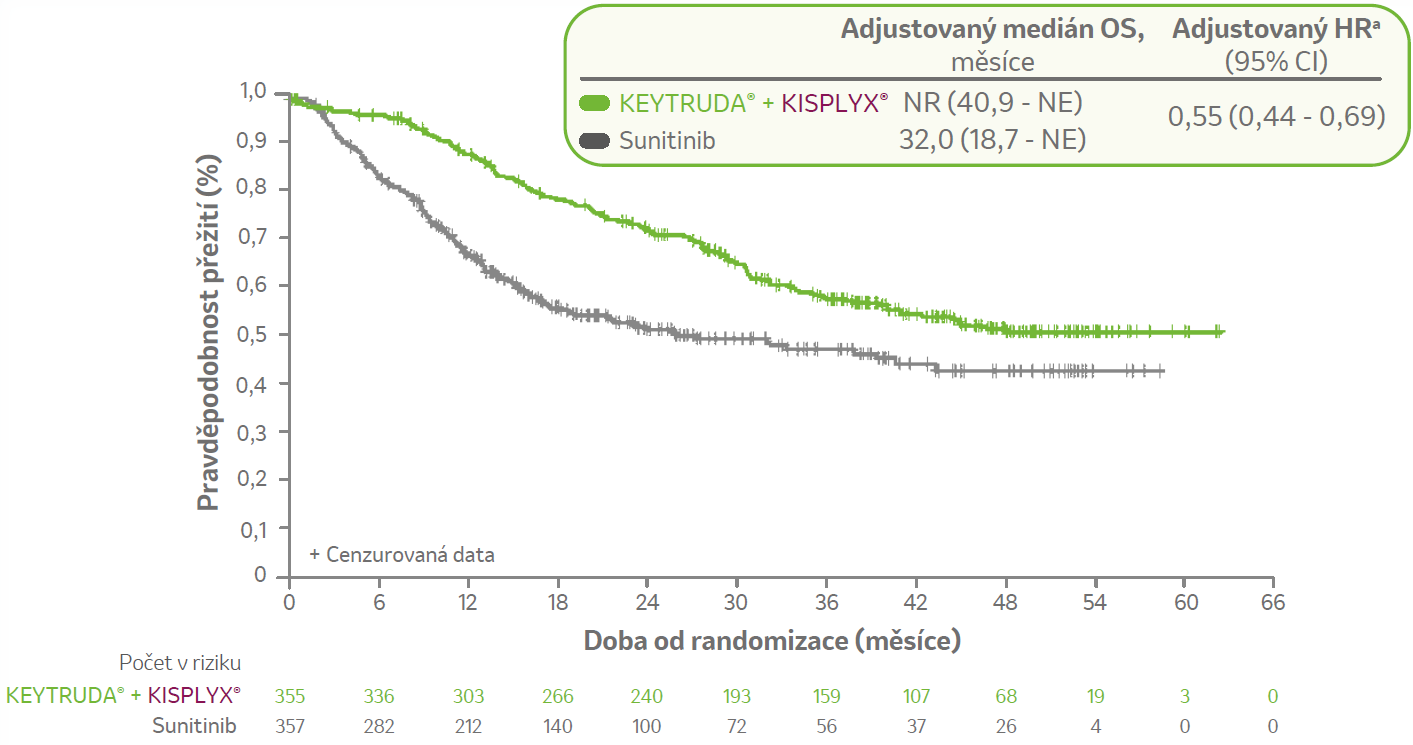
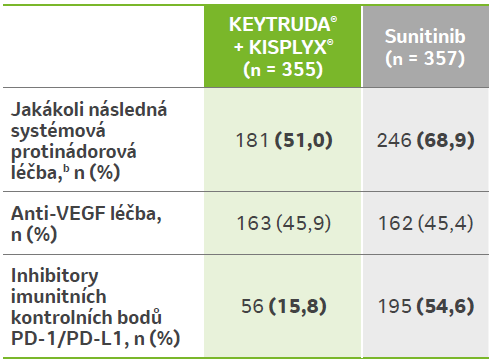
Pro post hoc analýzu OS byla použita metoda dvoufázového odhadu za účelem adjustace od dopadu nevyváženosti v následných léčbách protinádorovými přípravky mezi léčebnými skupinami.1
a Metoda dvoufázového odhadu post hoc pro adjustaci celkového přežití o případné vlivy následné léčby protinádorovými přípravky.1
b Během následného sledování přežití.1
Analýza podskupin z předem specifikované finální analýzy OS ze studie KEYNOTE-581/CLEAR1
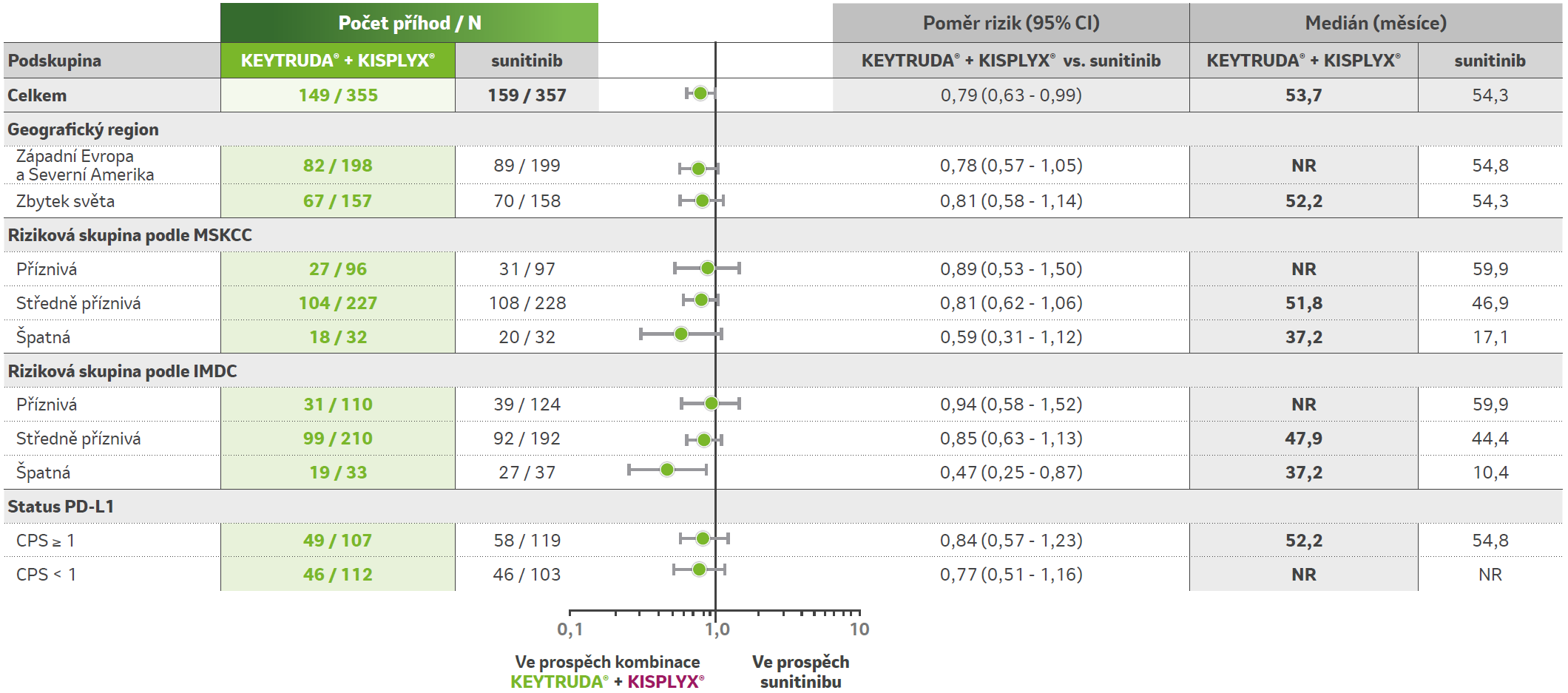
- Datum uzávěrky dat: 31. července 20221
- 23 měsíců dalšího sledování po primární analýze1
- Riziková skupina podle IMDC nebyla stratifikačním faktorem, relevantní data byla odvozena programově.1
Medián doby sledování (IQR) pro OS byl 49,8 měsíce (41,4 – 53,1) ve skupině léčené kombinací přípravků KEYTRUDA® + KISPLYX® a 49,4 měsíce (41,6 – 52,8) ve skupině léčené sunitinibem.1
Téměř 4x více pacientů dosáhlo kompletní odpovědi s kombinovanou léčbou přípravků KEYTRUDA® + KISPLAX® vs. sunitinib
Superiorní ORR v porovnání se sunitinibem1
Míry odpovědi z předem specifikované finální analýzy OS ze studie KEYNOTE-581/CLEAR.1
Celkový počet léčebných odpovědí1
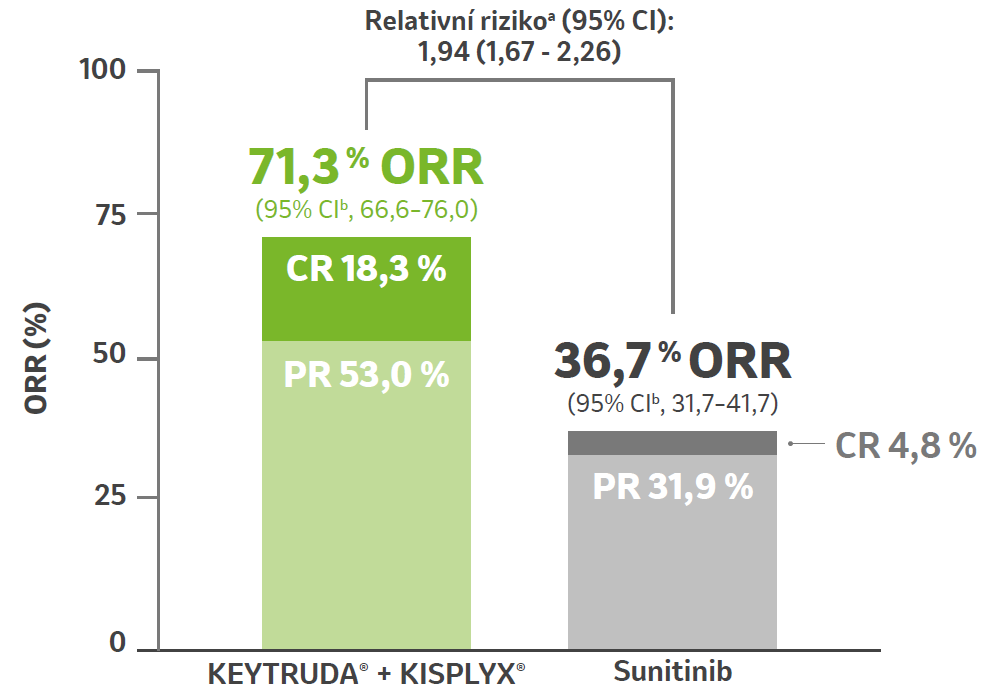
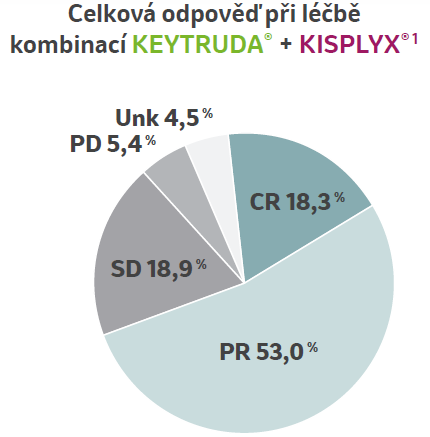
Míra CR činila 18,3 % při léčbě kombinací přípravků KEYTRUDA® + KISPLYX® oproti 4,8 % při léčbě sunitinibem.1
Součet procent nemůže být 100 kvůli zaokrouhlování.
Medián doby sledování (IQR) pro OS byl 49,8 měsíce (48,8–50,4) ve skupině léčené kombinací přípravků KEYTRUDA® + KISPLYX® a 49,4 měsíce (48,1–50,1) ve skupině léčené sunitinibem.1
a Relativní riziko bylo vypočteno Cochran-Mantel-Haenszelovou (CMH) metodou se stratifikací podle stratifikačních faktorů IxRS.1
b 95% CI byly určeny metodou normální aproximace.1
Medián trvání odpovědi (DOR) byl 26,7 měsíce v rameni KEYTRUDA® + KISPLYX® vs 14,7 měsíce v rameni se sunitinibem1,d
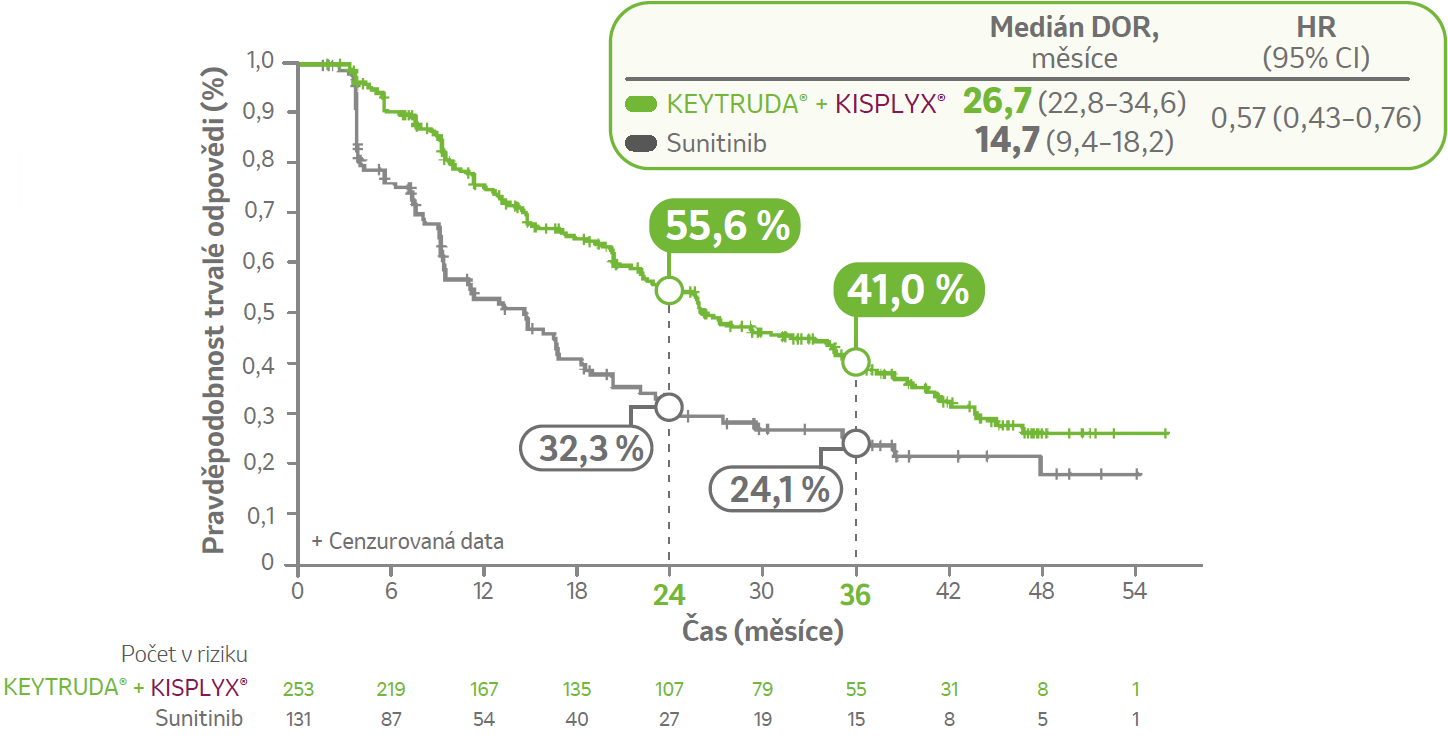


d DOR bylo podle IIR podle RECIST v1.1.1
e Téměř CR se týká pacientů s částečnou odpovědí, u kterých byla zjištěna maximální redukce nádoru ≥ 75 %.1
95% Cl byly stanoveny odhadem pomocí generalizované Brookmeyer-Crowley metody. Poměr rizik byl stanoven na základě Coxova modelu proporcionálních rizik s léčebnou skupinou jako faktorem; pro vazby byla použita Efronova metoda se stratifikací podle geografického regionu (region 1: západní Evropa a Severní Amerika, region 2: zbytek světa) a prognostických skupin MSKCC (příznivé, středně příznivé a špatné) in IXRS. 95% CI byly stanoveny metodou normální aproximace.
Reference:
1 Motzer RJ, Porta C, Eto M, et al. Final prespecified OS analysis of CLEAR: 4-year follow up of lenvatinib plus pembrolizumab vs sunitinib in patients with advanced renal cell carcinoma. Slide deck (Abstract #4502) presented at: American Society of Clinical Oncology (ASCO) Annual Meeting; June 2-6, 2023; Chicago, Illinois, USA.
2 SPC přípravku KEYTRUDA® na www.sukl.cz.